Síguenos en Nuestras Redes Sociales
–La compañía sigue en pie con los planes de reportar los datos del ensayo ELEVATE-44-201 de la Cohorte 1 en el segundo trimestre de 2026 y de la Cohorte 2 para finales de 2026–
–La compañía sigue en pie con los planes de reportar los datos del ensayo ELEVATE-45-201 de la Cohorte 1 a mediados de 2026–
–El Comité Independiente de Monitoreo de Datos recomendó iniciar la Cohorte 1 con un aumento de dosis de 12 mg./kg. en el estudio ELEVATE-44-201–
–Se espera tener reserva de liquidez en el tercer trimestre de 2027 con $296 millones en liquidez, activos líquidos equivalentes y valores negociables a partir del 31 de diciembre de 2025–
BOSTON, 26 de febrero de 2026 (GLOBAL NEWSWIRE) – Entrada Therapeutics, Inc. (Nasdaq: TRDA) el día de hoy reportó resultados financieros para el cuarto trimestre y el año completo que finalizó el 31 de diciembre de 2025, y resaltó algunas actualizaciones recientes sobre sus negocios.
“Hemos comenzado el año 2026 con gran impulso, incluyendo una recomendación positiva del Comité Independiente de Monitoreo de Datos (DMC, por sus siglas en inglés) para iniciar la segunda cohorte del ensayo ELEVATE-44-201 con un aumento de dosis de 12 mg./kg. En los próximos meses, compartiremos múltiples lecturas clínicas, incluyendo datos de las primeras cohortes de pacientes de los estudios ELEVATE-44-201 y ELEVATE-45-201, así como la segunda cohorte de pacientes del estudio ELEVATE-44-201 más adelante en el año. Confiamos en que estos resultados continúen disminuyendo el riesgo de nuestro portafolio neuromuscular completo,” dijo Dipal Doshi, Director Ejecutivo de Entrada Therapeutics. “Estamos también avanzando en nuestro portafolio en desarrollo creciente de medicina genética, con el nombramiento de la terapia ENTR-801 para el tratamiento potencial del síndrome de Usher tipo 2A y el nombramiento planificado de un segundo candidato clínico para enfermedades de la retina heredadas, esperado para más adelante este año. Con la reserva de liquidez en el tercer trimestre de 2027, creemos que estamos bien posicionados para continuar expandiendo nuestra línea de desarrollo única de medicina terapéutica intracelular.
Puntos sobresalientes corporativos recientes
Línea de desarrollo en etapa clínica. Entrada continúa avanzando en múltiples programas clínicos para personas con distrofia muscular de Duchenne (DMD) en el Reino Unido, la Unión Europea y Estados Unidos. En 2026, la compañía espera contar con cuatro programas en etapa clínica en su línea de DMD (ENTR-601-44, ENTR-601-45, ENTR-601-50 y ENTR-601-51), complementando el progreso clínico en curso de su colaboración en la distrofia miotónica tipo 1 (DM1) (VX-670) con Vertex.
- ELEVATE-44-201: Dosis completa de la Cohorte 1 de la parte de dosis múltiples ascendentes (MAD, por sus iniciales en inglés) del estudio global de Fase 1/2 ENTR-601-44 en pacientes ambulatorios que viven con DMD que son susceptibles a la omisión del exón 44. Un Comité Independiente de Monitoreo de Datos (DMC, por sus siglas en inglés) ha revisado los datos a la fecha de ocho pacientes inscritos en la Cohorte 1 y recomendó iniciar la Cohorte 2 con un aumento de dosis de 12 mg./kg. sin ningúna modificación de protocolo. Todos los participantes de la Cohorte 1 han pasado la parte abierta del estudio de Fase 2. La compañía sigue en pie para reportar datos de la Cohorte 1 (6 mg./kg.) para finales del año 2026, y los datos de la Cohorte 2 (12 mg./kg.) para finales del año 2026, y datos de la Cohorte 3 (hasta 18 mg./kg.) para seguir. Entrada pretende abrir una cohorte de expansión más adelante este año para aumentar el número de participantes tratados en el estudio ELEVATE-44-201, pues este estudio está diseñado para respaldar una aprobación acelerada en EE. UU. En diciembre de 2025, la Administración de Alimentos y Medicamentos de EE. UU. (FDA, por sus siglas en inglés) otorgó la Designación de Enfermedad Pediátrica Rara a la terapia ENTR-601-44.
- ELEVATE-44-102: la compañía cree que sería mejor iniciar este estudio clínico, en la población de pacientes adultos desatendidos con la enfermedad avanzada, en la dosis de inicio más alta que se recomiende. Tras una revisión de la seguridad, los datos de farmacocinética y farmacodinámica del estudio ELEVATE-44-201 en el Reino Unido y la Unión Europea en el segundo trimestre de 2026, la compañía planea volver a hablar con la FDA sobre el aumento de las dosis planificadas en este estudio clínico. Como tal, la compañía proporcionará una actualización sobre el diseño del estudio clínico y el tiempo tras los diálogos con la FDA.
- ELEVATE-45-201: Inició la dosis en pacientes en el ensayo clínico de MAD global de Fase 1/2 de la terapia ENTR-601-45 en pacientes ambulatorios que viven con DMD que son susceptibles a la omisión del exón 45. La compañía sigue en pie con los planes de reportar datos de la Cohorte 1 (5 mg/kg.) a mediados de 2026, con datos de la Cohorte 2 y Cohorte 3 (hasta 10 mg./kg. y 15 mg./kg., respectivamente) para seguimiento.
- ELEVATE-50-201: la compañía recibió la autorización regulatoria de la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA, por sus siglas en inglés) y el Comité de Ética en Investigación para comenzar un estudio clínico de MAD de Fase 1/2 de la terapia ENTR-601-50 en pacientes ambulatorios que viven con DMD que son susceptibles a la omisión del exón 50. La compañía espera enviar solicitudes regulatorias y obtener autorizaciones en la Unión Europea para la terapia ENTR-601-50 para finales del año 2026.
- ENTR-601-51: La compañía espera enviar solicitudes regulatorias globales para la terapia ENTR-601-51 en 2026.
- VX-670: Vertex continúa inscribiendo y dosificando la porción de MAD del ensayo clínico global de Fase 1/2 de la terapia VX-670 en personas con DM1. El estudio evalúa tanto la seguridad y eficacia y sigue con los planes de completar la inscripción y dosificación a mediados de 2026.
Expandiendo la línea de desarrollo preclínico: La compañía ha generado datos preclínicos convincentes de los programas enfocados en las enfermedades oculares y metabólicas. La línea de desarrollo incluye el avance de dos programas novedosos basados en oligonucleótidos para el tratamiento potencial de enfermedades de la retina heredadas, donde existen muchas necesidades por cubrir. El primer candidato ocular, ENTR-801, para el potencial tratamiento del síndrome de Usher tipo 2A (USH2A) fue anunciado en diciembre de 2025. La compañía planea anunciar un segundo candidato para la enfermedad ocular en la segunda mitad de 2026.
Próxima Conferencia con Inversores
- 46ª Conferencia Anual sobre Atención Sanitaria de TD Cowen, Boston, Massachusetts, 3 de marzo de 2026.
Resultados financieros del Cuarto trimestre y Año completo de 2025
Situación de liquidez: la liquidez, equivalentes y valores comerciales fueron de $295.7 millones al 31 de diciembre de 2025 en comparación con los $420.0 millones al 31 de diciembre de 2024. La disminución se debió principalmente al efectivo utilizado para financiar las operaciones. Basados en planes operacionales actuales, la compañía cree que su liquidez, equivalentes y valores comerciales al 31 de diciembre de 2025 serán suficientes para financiar sus operaciones en el tercer trimestre de 2027.
Ingresos por colaboración: los ingresos por colaboración fueron $1.3 millones para el cuarto trimestre de 2025 y $25.4 millones para el año completo de 2025, en comparación con los $37.4 millones y $210.8 millones para los mismos períodos en 2024. Esta disminución se atribuye principalmente a la completación sustancial del plan de actividades de investigación en colaboración asociadas con VX.670 durante el primer trimestre de 2025.
Gastos por Investigación y desarrollo (I&D): los gastos por I&D fueron de $34.0 millones para el cuarto trimestre y $142.3 millones para el año completo de 2025, en comparación con los $33.4 millones y $125.3 millones para los mismos periodos en 2024. El aumento se debe principalmente a los costos adicionales incurridos en relación a los programas para la DMD de la compañía, así como a costos más elevados de personal (incluyendo la compensación no monetaria basada en acciones).
Gastos generales y administrativos (G&A): los gastos por G&A fueron de $9.6 millones para el cuarto trimestre y $41.1 millones para el año completo de 2025, en comparación con los $9.9 millones y $38.5 millones para los mismos periodos en 2024. El aumento anual se debió principalmente a los costos más elevados de personal (incluyendo la compensación no monetaria basada en acciones).
Ingresos netos (pérdidas): la pérdida neta fue de $(39.2) millones para el cuarto trimestre de 2025 y $(143.8) millones para el año completo de 2025, en comparación con un ingreso neto de $1.1 millones y $65.6 millones para los mismos periodos en 2024.
Sobre Entrada Therapeutics
Entrada Therapeutics es una compañía biofarmacéutica de fase clínica que tiene por objetivo transformar las vidas de pacientes al establecer medicinas de clase nueva que involucran objetivos intracelulares que por mucho tiempo han sido consideradas inaccesibles. A través de enfoques propios, versátiles y modulares, Entrada está avanzando en un portafolio de desarrollo robusto de medicina genética para el potencial tratamiento de enfermedades de la retina hereditarias y neuromusculares, entre otras. Los programas de oligonucleótidos líderes de la Compañía están en desarrollo para el potencial tratamiento de las personas que viven con distrofia muscular de Duchenne que son susceptibles a la omisión de los exones 44, 45, 50 y 51. Entrada ha colaborado para desarrollar un programa en etapa clínica, VX-670, para la distrofia miotónica tipo 1.
Para más información sobre Entrada, por favor visite nuestro sitio web:
www.entradatx.com, y síganos en LinkedIn.
Declaraciones a futuro
Este comunicado de prensa contiene declaraciones a futuro expresas e implícitas que involucran riesgos e incertidumbres sustanciales. Todas las declaraciones, aparte de las declaraciones de hechos históricos, contenidas en este comunicado de prensa, incluyendo declaraciones en referencia a la estrategia de Entrada, operaciones futuras, prospectos y planes, objetivos de manejo, la validación y diferenciación del enfoque de Entrada y la plataforma de EEV y su habilidad para ofrecer un tratamiento potencial para pacientes, expectativas en referencia al estudio clínico de MAD de Fase 1/2 de Entrada para la terapia ENTR-601-44 incluyendo los tiempo de los datos de la Cohorte 1 en el segundo trimestre de 2026, de la cohorte 2 para finales de año, y de la cohorte 3 para seguimiento, expectativas en referencia al inicio del estudio clínico planificado ELEVATE-44-102 en EE. UU. incluyendo los planes para volver a hablar con la FDA sobre el aumento de dosis planeadas, expectativas en referencia al estudio clínico de MAD 1/2 de Entrada para la terapia ENTR-601-45, incluyendo los tiempo de los datos de la Cohorte 1 a mediados de 2026, con los datos de la Cohorte 2 y Cohorte 3 para seguimiento, expectativas en relación al tiempo de los archivos regulatorios en la Unión Europea para el estudio clínico de MAD de Fase 1/2 de la terapia ENTR-601-50 para finales de año 2026, expectativas en referencia al tiempo para los archivos regulatorios y autorización para el estudio clínico planificado de la terapia ENTR-601-51 en 2026, la habilidad para reclutar y completar los ensayos clínicos globales de Fase 2 de las terapias ENTR-601-22, ENTR-601-45, ENTR-601-50 y ENTR-601-51, los beneficios terapéuticos potenciales de los productos candidatos de EEV de Entrada y la habilidad de avanzar en los candidatos terapéuticos en indicaciones más allá de las enfermedades neuromusculares, incluyendo pero no limitando a enfermedades oculares, expectativas en referencia al tiempo de nominación de un segundo candidato clínico para enfermedades oculares en la segunda mitad de 2026, el continuo desarrollo y avance de las terapias ENTR-601-44, ENTR-601-45, ENTR-601-50, y ENTR-601-51 para el tratamiento potencial de la DMD y ENTR-601-801 para el potencial tratamiento del síndrome de Usher tipo 2A y el producto candidato colaborador VX-67’ para el tratamiento potencial de la DM1, expectativas en referencia al progreso y éxito de la colaboración de Entrada con Vertex, incluyendo la completación de la inscripción y dosificación de la porción de MAD en el estudio global de Fase ½ del programa VX-670 a mediados de 2026, la habilidad de continuar expandiendo y desarrollando programas y modalidades ter, incluyendo programas de omisión de exón más adelante, y los recursos de liquidez suficientes en el tercer trimestre de 2027, constituyen las declaraciones a futuro dentro del significado de la Ley de Reforma de los Litigios sobre Valores Privados de 1995. Las palabras “anticipar”, “creer”, “continuar”, “podría”, “estimar”, “esperar”, “pretender”, “poder”, “puede”, “objetivo”, “en curso”, “plan”, “predecir”, “proyectar”, “potencial”, “debería”, “sería”, o la forma negativa de estos términos, u otra terminología comparable son para identificar declaraciones a futuro, aunque no todas las declaraciones a futuro contienen estas palabras identificables. Entrada podría no lograr estos planes, intenciones, o expectativas mostradas en estas declaraciones a futuro, y usted no debería confiar completamente en estas declaraciones a futuro. Los resultados o eventos reales podrían diferir materialmente de estos planes, intenciones, o expectativas mostradas en estas declaraciones a futuro como resultado de varios factores importantes, incluyendo: incertidumbres inherentes a la identificación y desarrollo de productos candidatos, incluyendo la realización de actividades de investigación y la iniciación y completación de estudios preclínicos y clínicos; incertidumbres como la disponibilidad y el tiempo de los resultados de estudios preclínicos y clínicos, el tiempo de la habilidad de Entrada para enviar y obtener autorización regulatoria e iniciar estudios clínicos, ya sea que los resultados de estudios preclínicos o clínicos sean predictivos de los resultados de estudios preclínicos o clínicos posteriores; ya sea que los recursos de liquidez de Entrada sean suficientes para financiar los gastos previstos y no previstos de la compañía y los requerimientos para obtener capital; así como los riesgos e incertidumbres identificados en los archivos de Entrada con la Comisión de Bolsa y Valores (SEC, por sus siglas en inglés), incluyendo la Forma 10-K más reciente de la compañía y en archivos subsecuentes de Entrada que pudiera hacer con la SEC. Además, las declaraciones a futuro incluidas en este comunicado de prensa representan las ideas de Entrada a la fecha del mismo comunicado de prensa. Entrada anticipa que los eventos y desarrollos subsecuentes harán que estas ideas cambien. Sin embargo, aunque Entrada puede decidir actualizar estas declaraciones a futuro en algún momento en el futuro, hace saber que no tiene obligación de hacerlo. Estas declaraciones a futuro no deberían ser completamente confiables para representar las ideas de Entrada a cualquier fecha subsecuente a la fecha de este comunicado de prensa.
ENTRADA THERAPEUTICS, INC.
Estados financieros consolidados condensados (sin auditar)
(En miles, excepto las cantidades de acción y por acción)
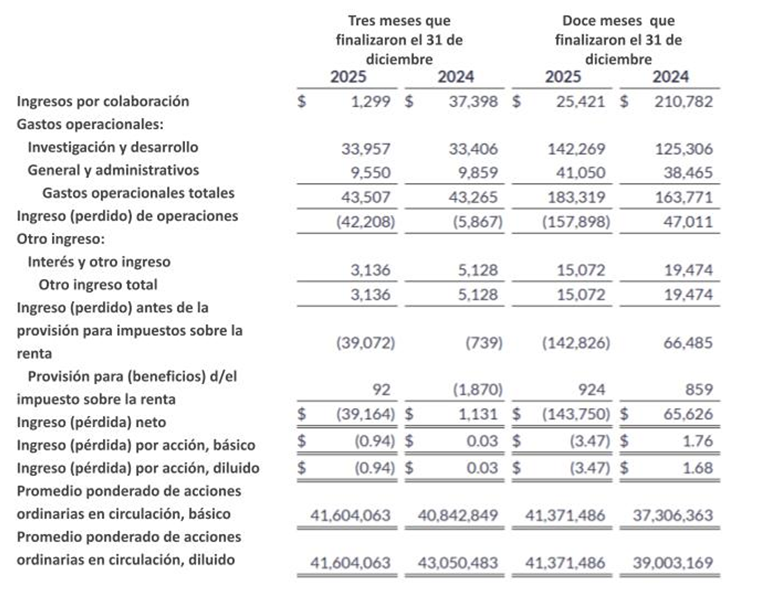
ENTRADA THERAPEUTICS, INC.
Estados financieros consolidados condensados (sin auditar)
(En miles)

Contacto con Inversores
Karla MacDonald
Directora de Asuntos Corporativos
Defensa de Pacientes
Sarah Friedhoff
Jefa de Defensa de Pacientes
Contacto con Medios de comunicación
Megan Prock
McGrath CTD Comms, LLC
Esta publicación está escrita en español para promover el acceso de la comunidad a información y actualizaciones. La información que se comparte tiene como objetivo el interés y la concientización general y, por lo tanto, no debe ser considerada ni interpretada como consejo médico o legal. Se trata de información publicada abiertamente. La Fundación Akari no promociona ninguna empresa, producto o tratamiento específico. Le recomendamos que consulte la fuente original y tome decisiones informadas.
Para leer el comunicado de prensa original en inglés consulte:
Si desea saber más información acerca de este comunicado de prensa, contáctese directamente con la fuente original de este comunicado.

