Síguenos en Nuestras Redes Sociales
10 de marzo de 2026
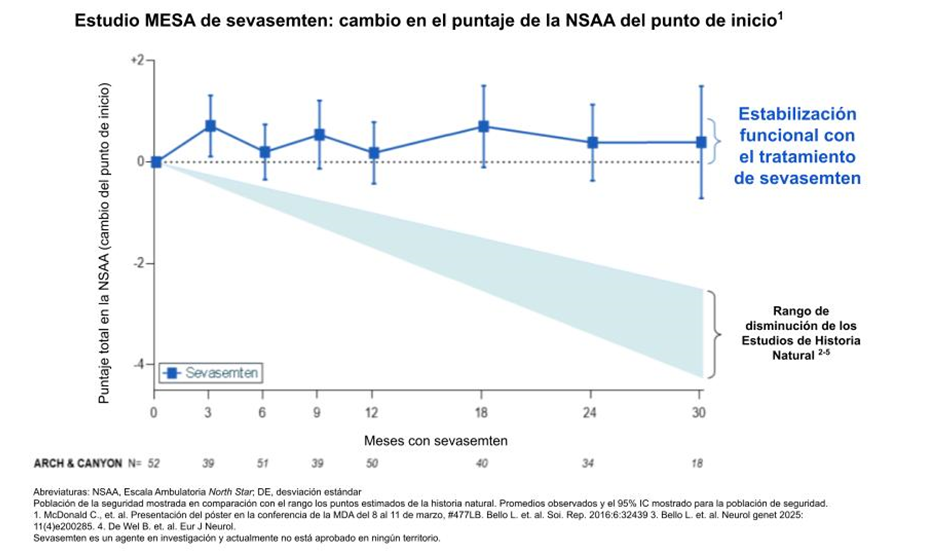
– Los datos del estudio META muestran estabilización de la función en participantes que toman sevasemten frente a la disminución funcional prevista que se observó en los estudios de historia natural de Becker. –
– Los datos refuerzan hallazgos clínicos previos de sevasemten en Becker, una enfermedad rara sin tratamientos aprobados. –
– La cohorte pivotal controlada con placebo GRAND CANYON sigue en marcha para su lectura en el cuarto trimestre de 2026. –
BOULDER, Colo., 10 de marzo de 2026 / PRNewswire/ — Edgewise Therapeutics, Inc. (Nasdaq: EWTX), una compañía biofarmacéutica líder en enfermedades musculares, presentó el día de hoy en la Conferencia Clínica y Científica 2026 de la MDA los datos a largo plazo de su estudio de extensión abierto MESA de sevasemten en la distrofia muscular de Becker (Becker), una enfermedad genética devastadora que no cuenta con intervenciones terapéuticas aprobadas. Los datos mostraron que los participantes que toman sevasemten experimentaron estabilización de la función por poco más de 3.5 años, en contraste con la disminución funcional prevista de los datos de historia natural de Becker.
“Por primera vez con un agente en investigación, estamos viendo datos a largo plazo donde las personas con Becker se mantienen estables de cara a una enfermedad que hemos visto que, de otro modo, conduciría a una disminución funcional significativa,” dijo Joanne Donovan, Dra. en Medicina, PhD, Directora Médica de Edgewise Therapeutics. “Nos mantenemos sobre la marcha para entregar los datos pivotales del ensayo GRAND CANYON de sevasemten y avanzar hacia la primera solicitud de comercialización para el tratamiento de Becker.”
El estudio MESA es una extensión abierta que evalúa la seguridad, tolerabilidad, y eficacia a largo plazo de sevasemten en adultos y adolescentes con Becker previamente tratados con sevasemten en ensayos clínicos. Casi todos los participantes elegibles (99%) de estudios de sevasemten previos (incluyendo ARCH, CANYON/GRAND CANYON, y DUNE) escogieron inscribirse en el estudio de extensión abierto MESA.
Los hallazgos clave reportados después de la participación de 12 meses en los estudios ARCH y CANYON, y seguimientos posteriores en el estudio MESA son los siguientes:
- Estabilización sostenida por 3.5 años: los puntajes funcionales en la Escala Ambulatoria North Star (NSAA, por sus siglas en inglés) de los participantes en los estudios ARCH y CANYON tratados con sevasemten se mantuvieron estables después de 3.5 y 2 años, respectivamente. Los participantes en el estudio CANYON con placebo quienes se pasaron al estudio MESA también tuvieron puntajes funcionales en la NSAA que tendieron a la alza durante el primer año después de cambiarse a sevasemten.
- Diferencia de los estudios de historia natural de Becker: una vez que la disminución funcional en Becker comienza, su curso normalmente continúa junto con la trayectoria descendente. Los múltiples estudios de historia natural en Becker reportan puntajes en la NSAA disminuyendo por un promedio de 1.0 a 1.7 puntos anualmente; esto equipara a una disminución funcional en promedio esperada de 3.0 a 5.1 puntos por 3 años. 1-4
- En el estudio MESA, los puntajes en la NSAA observados en el brazo (grupo) de tratamiento con sevasemten difirieron marcadamente de las disminuciones de los estudios de historia natural previstos:
- El estudio CANYON por 2 años: +0.1 de mejora (tratados) frente a -2.9 de disminución (historia natural prevista)
- El estudio ARCH por 3.5 años: +0.1 de mejora (tratados) frente a -5.3 de disminución (historia natural prevista)
Sevasemten, un inhibidor de miosina esquelética rápida en investigación diseñado para proteger a los músculos del daño inducido por la contracción, continuó mostrando un perfil de seguridad favorable en el estudio MESA con exposición a largo plazo por más de 3 años.
La Compañía espera anunciar los resultados principales de la cohorte pivotal controlada con placebo, GRAND CANYON, en el cuarto trimestre de 2026. Si los datos son positivos, la Compañía avanzará con sevasemten hacia una solicitud para comercialización para buscar la aprobación como la primera terapia orientada a esta población desatendida.
Sobre la distrofia muscular de Becker
Becker es un trastorno neuromuscular raro, genético, relacionado al cromosoma X que afecta predominantemente a los hombres. Las mutaciones en el gen de la distrofina resultan en daño muscular inducido por la contracción, conduciendo a la pérdida muscular irreversible y progresiva, el declive de la función motora, y a la reducción de la esperanza de vida. Los síntomas pueden comenzar a cualquier edad, habiendo deterioro funcional continuo a lo largo de la vida. Actualmente, no hay terapias aprobadas en el mercado que traten la enfermedad subyacente.
Sobre Sevasemten y el estudio MESA
Sevasemten es una terapia administrada por vía oral que modula selectivamente la contracción muscular esquelética rápida para reducir el daño en las distrofias musculares. Sevasemten representa un mecanismo de acción novedoso diseñado para limitar de forma selectiva el daño muscular exagerado causado por la ausencia o pérdida de distrofina funcional. Sevasemten está siendo estudiada en ensayos clínicos en fase avanzada de la distrofia muscular de Becker y Duchenne.
El estudio MESA es de extensión abierta, y que evalúa la seguridad, tolerabilidad, y eficacia a largo plazo de sevasemten en adultos y adolescentes con Becker previamente tratados en ensayos clínicos de sevasemten. Para más información, vea el póster del estudio MESA 2026 de la MDA haciendo click aquí y en la página clinicaltrials.gov (NCT06066580).
Sobre Edgewise Therapeutics
Edgewise Therapeutics es una compañía biofarmacéutica líder en enfermedades musculares que desarrolla terapias novedosas para distrofias musculares y condiciones cardiacas severas. La profunda experiencia de la Compañía en fisiología muscular impulsa una nueva generación de novedosas terapias. Sevasemten es un inhibidor de miosina esquelética rápida administrado oralmente en ensayos clínicos de última fase para las distrofias musculares de Becker y Duchenne. EDG-7500 es un novedoso modulador del sarcómero cardíaco para el tratamiento de la miocardiopatía hipertrófica actualmente en desarrollo clínico de Fase 2. EDG-15400 es un novedoso modulador del sarcómero cardíaco para el tratamiento de la insuficiencia cardíaca, actualmente en desarrollo clínico de Fase 1. Todo el equipo de Edgewise se dedica a nuestra misión: cambiar las vidas de pacientes y familias afectados por enfermedades musculares severas. Para saber más, puede visitar: www.edgewisetx.com o seguirnos en LinkedIn, X, Facebook e Instagram.
Referencias
- Bello L, et al. Sci Rep. 2016;6:32439.
- Bello L, et al. Neurol Genet. 2025;11(4)e200285.
- De Wel B, et al. Eur J Neurol. 2024; 31(7):e16282.
- Schrama EJ, et al. Neurology. 2025;105(7):e214071.
Nota aclaratoria sobre declaraciones a futuro
Este comunicado de prensa contiene declaraciones a futuro, tal como se define dicho término en la Sección 27A de la Ley de Valores de 1933 y Sección 21E de la Ley de Intercambio de Valores de 1934. Las declaraciones en este comunicado de prensa que no son meramente históricas son declaraciones a futuro. Dichas declaraciones a futuro incluyen, entre otras cosas, declaraciones sobre el potencial y expectativas relacionadas con sevasemten; declaraciones sobre los hitos y expectativas de Edgewise en relación a sus ensayos clínicos y desarrollo clínico de sevasemten, incluyendo el tiempo estimado de la lectura de la cohorte pivotal para el ensayo GRAND CANYON; declaraciones en relación al posible resultado del ensayo GRAND CANYON; declaraciones en relación a la habilidad de Edgewise de obtener aprobación regulatoria para sevasemten; declaraciones en relación al potencial de sevasemten de ser la primera terapia aprobada para Becker; y declaraciones hechas por el Director Médico de Edgewise. Palabras como “cree”, “anticipa”, “planea”, “espera”, “pretende”, “será”, “objetivo”, “potencial”, y expresiones similares, están orientadas a identificar declaraciones a futuro. Las declaraciones a futuro contenidas aquí se basan en las expectativas actuales de Edgewise e involucran suposiciones que pudieran nunca materializarse o probarse incorrectas. Los resultados reales pudieran diferir materialmente de aquellos proyectados en declaraciones a futuro debido a numerosos riesgos e incertidumbres, incluyendo pero no limitado a: riesgos asociados con el historial operante limitado de Edgewise; sus productos en etapas tempranas de desarrollo y no contar con productos aprobados para venta comercial; riesgos asociados con la falta de generación de réditos de Edgewise a la fecha; la capacidad de Edgewise de lograr objetivos relacionados con el descubrimiento, desarrollo y comercialización de sus productos candidatos, en caso de ser aprobados; la necesidad de Edgewise de capital adicional sustancial para financiar sus operaciones; la dependencia sustancial de Edgewise del éxito de sevasemten; la capacidad de Edgewise de desarrollar y comercializar sevasemten; riesgos relacionados con no demostrar seguridad y eficacia en los ensayos clínicos de Edgewise de sus productos candidatos; riesgos relacionados con causar eventos adversos severos, toxicidades, o algún otro efecto secundario no deseado con los productos candidatos de Edgewise; el resultado de las pruebas preclínicas y ensayos clínicos tempranos resultaran no siendo predictivos del exito de ensayos clínicos posteriores y que los riesgos relacionados con los resultados de los ensayos clínicos de Edgewise no cumplieran los requisitos de las autoridades regulatorias; retrasos o dificultades en la inscripción y/o mantenimiento de pacientes en ensayos clínicos; riesgos relacionados a la incapacidad de capitalizar en otras indicaciones o productos candidatos, riesgos relacionados con la competencia; riesgos relacionados con cambios en los datos provisionales, importantes y preliminares de los ensayos clínicos de Edgewise, conforme más datos de pacientes se encuentren disponibles; riesgos relacionados con no cumplir el desarrollo en una propia plataforma de descubrimiento de fármacos; riesgos relacionados con la exposición a riesgos adicionales se desarrollamos sevasemten en conexión con otras terapias; riesgos relacionados con la producción de medicinas por manufactureras de terceras personas para Edgewise; riesgos relacionados con cambios en los métodos de manufacturación o formulación de productos candidatos; riesgos relacionados con no lograr aceptación adecuada en el mercado; riesgos relacionados a que la población de pacientes de nuestros productos candidatos sea pequeña; riesgos relacionados a que los procesos de aprobación regulatoria por parte de autoridades locales y extranjeras sean largos, inherentemente impredecibles, y que consuman tiempo; riesgos relacionados con interrupciones en la FDA, la SEC, y otras agencias gubernamentales; riesgos relacionados con la capacidad de Edgewise de atraer y retener jefes ejecutivos y empleados altamente calificados; la capacidad de Edgewise de obtener y mantener protegida la propiedad intelectual de sus productos candidatos; la confianza de Edgewise en terceras personas; riesgos relacionados con adquisiciones futuras o colaboraciones estratégicas; riesgos relacionados a condiciones comerciales y económicas generales; y otros riesgos. La información sobre riesgos adicionales y precedentes se puede encontrar en la sección “Factores de riesgo” en documentos que Edgewise archiva de vez en cuando con la Comisión de Bolsa y Valores de EE. UU. Estas declaraciones a futuro se hacen a la fecha de este comunicado de prensa, y Edgewise no asume obligación alguna de actualizar las declaraciones a futuro, o de actualizar las razones de por las que los resultados reales pudieran diferir de aquellos proyectados en las declaraciones a futuro, a menos de ser requerido por la ley.
Este comunicado de prensa incluye hipervínculos a información que no se considera incorporada por referencia al presente comunicado.
Para ver el contenido original y descargar contenido multimedia: Edgewise Announces Positive Long-Term Sevasemten Data Demonstrating Sustained Functional Stabilization in Becker Muscular Dystrophy Through 3.5 Years of Follow-Up
FUENTE Edgewise Therapeutics
Esta publicación está escrita en español para promover el acceso de la comunidad a información y actualizaciones. La información que se comparte tiene como objetivo el interés y la concientización general y, por lo tanto, no debe ser considerada ni interpretada como consejo médico o legal. Se trata de información publicada abiertamente. La Fundación Akari no promociona ninguna empresa, producto o tratamiento específico. Le recomendamos que consulte la fuente original y tome decisiones informadas.
Para leer el comunicado de prensa original en inglés consulte:
Si desea saber más información acerca de este comunicado, contáctese directamente con la fuente original del mismo.

