Síguenos en Nuestras Redes Sociales
Querida Comunidad:
Nos gustaría compartir con ustedes una actualización: más de 1,000 personas que tienen distrofia muscular de Duchenne han sido tratados con DUVYZAT® (givinostat).
Este hito refleja más que sólo números. Refleja lo que es posible cuando una comunidad se une alrededor de un propósito compartido: aumentar las opciones de tratamiento para las personas con Duchenne.
Desde las etapas más tempranas de desarrollo, hasta donde estamos el día de hoy, las perspectivas, la retroalimentación, y la determinación de pacientes, familias, personal clínico, y defensores han marcado cada paso. Estamos satisfechos por contribuir al progreso, así como conscientes de la responsabilidad que ello conlleva.
Este es sólo un punto dentro de una trayectoria más larga, pues hay más qué hacer. Pero momentos como este nos recuerdan por qué continuamos escuchando de cerca, colaborando plenamente, y enfocados en hacer una diferencia significativa todos juntos.
Nuestro presidente Matt Trudeau redactó una publicación en el blog que compartimos a través de Facebook, donde reflexiona sobre la importancia de este hito. Agradeceríamos si consideraran seguirnos en Facebook, dar ‘like’ a la publicación, y compartirla con sus seguidores. Gracias por su defensa y liderazgo.
¿Qué es DUVYZAT?
DUVYZAT es una medicina recetada para el tratamiento de la distrofia muscular de Duchenne (DMD) en personas a partir de los 6 años y en adelante. No se sabe si DUVYZAT es segura y efectiva en menores de 6 años.
Información de Seguridad Importante
¿Cuál es la información más importante que debo saber sobre DUVYZAT?
- Conteo de plaquetas bajo en la sangre (trombocitopenia). Las plaquetas son importantes para la coagulación de sangre, por lo que tener pocas puede aumentar el riesgo de sangrado y de moretones. Su doctor revisará su conteo sanguíneo antes de comenzar a tomar DUVYZAT, así como de manera regular durante el tratamiento para encontrar posibles signos de trombocitopenia. Llame a su doctor inmediatamente si nota sangrado inusual o pequeñas marcas rojas o moradas en la piel.
- Niveles elevados de grasa (triglicéridos) en su sangre. Podría no presentar ningún síntoma, por lo que su doctor realizará pruebas de sangre antes de que empiece a tomar DUVYZAT, así como de manera regular durante el tratamiento para revisar sus niveles de triglicéridos.
- Heces acuosas (diarrea) y vómitos frecuentes. DUVYZAT puede causar vómito y diarrea de moderada a severa. Si hay diarrea, debe mantener un registro de la frecuencia y severidad de sus síntomas, beber suficientes líquidos, y contactar a su doctor.
- Si la trombocitopenia, los triglicéridos elevados, o la diarrea no se pueden tratar, su doctor puede controlar la dosis o detener el tratamiento con DUVYZAT de ser necesario.
Antes de tomar DUVYZAT, informe a su doctor de todas sus condiciones médicas, incluyendo:
- Cualquier problema en el corazón o medicamentos que tome que pudieran incrementar las probabilidades de ritmo cardíaco irregular.
- Cualquier problema de sangrado.
Informe a su doctor sobre todas las medicinas que toma, incluyendo las que son con receta, de venta libre, vitaminas, y suplementos herbales.
Tomar DUVYZAT junto con ciertas medicinas puede afectar una a la otra, además de que puede causar efectos secundarios serios. No empiece o deje de tomar otras medicinas sin hablarlo con su doctor.
¿Cuáles son los efectos secundarios posibles de DUVYZAT?
- Duvyzat puede causar efectos secundarios serios, incluyendo cambios en la actividad eléctrica de su corazón, llamada prolongación del QT. La prolongación del QT puede elevar el riesgo de desarrollar un tipo de ritmo cardíaco irregular conocido como Torsades de Pointes. Llame a su doctor inmediatamente si presenta desmayos, ritmo cardíaco irregular, se siente mareado, o pierde el conocimiento. Revise la sección titulada “¿Cuál es la información más importante que debo saber sobre DUVYZAT?” para conocer más sobre los efectos secundarios.
Los efectos secundarios más comunes (ocurriendo en >5% de los pacientes tratados con DUVYZAT) incluyen diarrea, dolor abdominal, niveles bajos de plaquetas, náuseas/vómito, niveles altos de triglicéridos, temperatura elevada/fiebre, dolores musculares, sarpullido, dolor de articulaciones, fatiga, estreñimiento, y menos apetito.
Éstos no son todos los efectos secundarios posibles de DUVYZAT. Para mayor información, pregunte a su doctor o farmaceuta.
Llame a su doctor para recibir un mayor asesoramiento médico sobre los efectos secundarios, los cuales también puede reportar a la FDA al 1-800-FDA-1088.
Por favor, revise la Información de receta completa (ver más abajo) y la Guía del Medicamento (ver más abajo).
DUVYZAT es una marca registrada de Italfarmaco S.p.A.
Atentamente,
Caroline Allen
Jefa de Defensa de los Pacientes en EE. UU.

c.allen@ITFTherapeutics.com
+1 (617) 599-2561
575 Virginia Road Concord, MA 01742
C-DUV-US-0538 08/2025

INFORMACIÓN DE RECETA COMPLETA
1. INDICACIONES Y USO
DUVYZAT está indicada para el tratamiento de la distrofia muscular de Duchenne (DMD) en pacientes de 6 años de edad y en adelante.
2. DOSIS Y ADMINISTRACIÓN
2.1 Evaluación y pruebas recomendadas antes de comenzar a tomar DUVYZAT
Obtenga y evalúe el conteo de plaquetas y triglicéridos de inicio previo a comenzar a tomar DUVYZAT [vea Advertencias y precauciones (5.1, 5.2)]. No comenzar a tomar DUVYZAT en pacientes con conteo de plaquetas menor que 150 x 109/L . Monitoree el conteo de plaquetas y triglicéridos como se recomiende durante el tratamiento para determinar si se necesitan modificaciones de las dosis [vea Dosis y administración (2.3)].
Además, en pacientes con enfermedad cardíaca subyacente o que tomen medicamentos en simultáneo que causan prolongación del intervalo QT, realizarse electrocardiogramas cuando se inicie el tratamiento con DUVYZAT, durante el uso simultáneo, y como se indique clínicamente [vea Dosis y administración (2.3), Advertencias y precauciones (5.4), e Interacciones con el medicamento (7.2)].
2.2 Dosis recomendada
La dosis recomendada de DUVYZAT se basa en el peso corporal y se administra de forma oral dos veces al día con alimentos (vea la Tabla 1) [vea Dosis y administración (2.4)].
Tabla 1: Dosis recomendada en pacientes de 6 años de edad y en adelante para el tratamiento de la DMD
| Peso土 | Dosis | Volumen de suspensión oral |
| 10 kg a menos de 20 kg | 22.2 mg dos veces al día | 2.5 ml dos veces al día |
| 20 kg a menos de 40 kg | 31 mg dos veces al día | 3.5 ml dos veces al día |
| 40 kg a menos de 60 kg | 44.3 mg dos veces al día | 5 ml dos veces al día |
| 60 kg o más | 53.2 mg dos veces al día | 6 ml dos veces al día |
2.3 Modificación de la dosis por reacciones adversas
Disminución de plaquetas, diarrea, aumento de triglicéridos
DUVYZAT puede causar reacciones adversas [vea Advertencias y precauciones (5.1, 5.2, 5.3)], lo que puede requerir de una modificación de dosis (vea Tabla 2) si ocurre algunas de las siguientes situaciones:
- Conteo de plaquetas <150 x 109 L verificado en dos evaluaciones con una semana de diferencia
o
- Diarrea severa o moderada
o
- Triglicéridos en ayunas >300 mg/dL verificados en dos evaluaciones con una semana de diferencia
Basada en la severidad de estas reacciones adversas, se debe considerar la interrupción del tratamiento previa a la modificación de la dosis.
Tabla 2: Modificaciones de la dosis para reacciones adversas en pacientes de 6 años de edad y en adelante para el tratamiento de la DMD
| Primera modificación de la dosis | Segunda modificación de la dosis | |||
Peso土 | Dosis | Volumen de suspensión oral | Dosis | Volumen de suspensión oral |
| 10 kg a menos de 20 kg | 17.7 mg dos veces al día | 2 ml dos veces al día | 13.3 mg dos veces al día | 1.5 ml dos veces al día |
| 20 kg a menos de 40 kg | 22.2 mg dos veces al día | 2.5 ml dos veces al día | 17.7 mg dos veces al día | 2 ml dos veces al día |
| 40 kg a menos de 60 kg | 31 mg dos veces al día | 3.5 ml dos veces al día | 26.6 mg dos veces al día | 3 ml dos veces al día |
| 60 kg o más | 39.9 mg dos veces al día | 4.5 ml dos veces al día | 15.4 mg dos veces al día | 4 ml dos veces al día |
土 Basado en el peso corporal real
* Si la reacción adversa persiste después de la primera modificación de la dosis, proceder a la segunda modificación de la dosis.
** Si la reacción adversa persiste después de la segunda modificación de la dosis, se debe suspender DUVYZAT.
Prolongación del intérvalo QTc
Suspenda DUVYZAT si el intervalo QTc es >500 ms o el cambio desde el inicio es >60 ms [vea Advertencias y precauciones (5.4) e Interacciones con el medicamento (7.2)].
2.4 Instrucciones de preparación y administración
Vea las Instrucciones de uso para mayor detalle.
- Antes de tomar, agite la suspensión DUVYZAT por al menos 30 segundos invirtiendo la botella 180o.
- Verifique visualmente la homogeneidad de la suspensión.
- Use una jeringa oral graduada para medir el volumen apropiado de la suspensión correspondiente a la dosis recetada de DUVYZAT.
- Administre de manera oral con la jeringa oral graduada que se incluye.
2.5 Dosis omitida
Si se les olvida tomar una dosis, los pacientes no deben tomar dosis dobles o extras.
3. FORMAS DE DOSIS Y CONCENTRACIONES
Suspensión oral: 8.86 mg/mL de givinostat como una suspensión de color blanco a blanquecino o ligeramente rosa, con sabor a durazno con crema.
4. CONTRAINDICACIONES
Ninguna.
5. ADVERTENCIAS Y PRECAUCIONES
5.1 Cambios hematológicos
Duvyzat puede causar trombocitopenia relacionada con la dosis y otros signos de mielosupresión, incluyendo hemoglobina baja y neutropenia.
En el estudio 1 [vea Estudios Clínicos (14)], se mostró trombocitopenia en 33% de los pacientes tratados con DUVYZAT en comparación con ningún paciente en el placebo. La disminución máxima de plaquetas se dio dentro de los primeros 2 meses de terapia y se mantuvo baja a lo largo del curso de la terapia. En algunos pacientes, la trombocitopenia se asoció con sangrados incluyendo epistaxis, hematomas, o contusiones. Los conteos bajos de plaquetas resultaron en una reducción de la dosis de DUVYZAT en el 28% de los pacientes. Los pacientes con conteos de plaquetas iniciales por debajo del límite normal fueron excluidos del estudio.
También se observó una disminución de la hemoglobina y de los neutrófilos en pacientes tratados con DUVYZAT en comparación con el placebo.
Monitoree los conteos sanguíneos cada 2 semanas durante los primeros 2 meses de tratamiento, en el mes 3, y luego cada 3 meses a partir de ahí. Modifique la dosis de DUVYZAT para la trombocitopenia confirmada [vea Dosis y administración (2.3)]. El tratamiento deberá ser suspendido permanentemente si las anormalidades empeoran a pesar de la modificación de la dosis. Si un paciente desarrolla signos o síntomas de trombocitopenia, obtenga un conteo de plaquetas tan pronto como sea posible, o suspenda la dosis hasta que se confirme el conteo de plaquetas.
5.2 Aumento de triglicéridos
DUVYZAT puede causar elevaciones en los triglicéridos. En el estudio 1 [vea Estudios Clínicos (14)], se presentó hipertrigliceridemia en el 23 % de los pacientes tratados con DUVYZAT (uno de los cuales tenía hipertrigliceridemia familiar), en comparación con el 7 % de los pacientes en el placebo. Los triglicéridos elevados (por ejemplo, niveles de más de 300 mg/dL) resultaron en la suspensión y condujeron a la modificación de la dosis en el 2% y 8 %, respectivamente, de los pacientes tratados con DUVYZAT.
Monitoree los triglicéridos al mes 1, los 3 meses, los 6 meses, y luego cada 6 meses a partir de ahí. Modifique la dosis si los triglicéridos en ayunas son verificados en > 300 mg/dL [vea Dosis y administración (2.3)]. El tratamiento con DUVYZAT deberá ser suspendido si los triglicéridos se mantienen elevados a pesar de la intervención en la dieta adecuada y un ajuste de dosis.
5.3 Problemas gastrointestinales
Los problemas gastrointestinales, incluyendo diarrea, náuseas/vómitos, y dolor abdominal fueron reacciones adversas comunes en la DMD en los ensayos clínicos de DUVYZAT. En el estudio 1, la diarrea se reportó en 37% de los pacientes tratados con DUVYZAT (con 1 caso severo reportado) en comparación con el 20% de los pacientes en el placebo. La diarrea usualmente se presentó dentro de las primeras semanas en que se inició el tratamiento con DUVYZAT.
Los vómitos y náuseas, a veces severas y normalmente presentándose durante el tratamiento con DUVYZAT, ocurrieron en el 32% de los pacientes tratados con DUVYZAT en comparación con el 18% de los pacientes en el placebo. Hubo dolor abdominal en el 34% de los pacientes tratados con DUVYZAT en comparación con el 25% de los pacientes en el placebo. Un caso de dolor abdominal fue serio.
Pueden considerarse también medicamentos antidiarreicos y antieméticos durante el tratamiento con DUVYZAT. Los líquidos y electrolitos deben reemplazarse conforme sea necesario para prevenir la deshidratación [vea Advertencias y precauciones (5.4)]. Modifique la dosis de DUVYZAT en pacientes con diarrea de moderada a severa, interrumpa el tratamiento si los síntomas importantes persisten [vea Dosis y administración (2.3)].
5.4 Prolongación del intervalo QTc
DUVYZAT puede causar prolongación del intervalo QTc [vea Farmacología clínica (12.2)]. Evite el uso de DUVYZAT en pacientes que están en mayor riesgo de arritmias ventriculares (incluyendo Torsades de Pointes), como aquellos con síndrome de intervalo QT largo congénito, arteriopatía coronaria, alteración electrolítica [vea Advertencias y precauciones (5.3)], el uso simultáneo de otros medicamentos conocidos por causar una prolongación del intervalo QT [vea Interacciones con el medicamento (7.2)]. Realizar electrocardiogramas previos a comenzar el tratamiento con DUVYZAT en pacientes con enfermedad cardíaca subyacente o en pacientes que toman medicamentos en simultáneo que causan prolongación del intervalo QT [vea Dosis y administración (2.1)].
6. REACCIONES ADVERSAS
Las siguientes reacciones adversas severas se describen a continuación y en otras partes de la etiqueta:
- Cambios hematológicos [vea Advertencias y precauciones (5.1)]
- Aumento de los triglicéridos [vea Advertencias y precauciones (5.2)]
- Problemas gastrointestinales [vea Advertencias y precauciones (5.3)]
- Prolongación del intervalo QTc [vea Advertencias y precauciones (5.4)]
6.1 Experiencia en ensayos clínicos
Debido a que los ensayos clínicos se llevan a cabo bajo condiciones ampliamente variables, los rangos de reacciones adversas observados en los ensayos clínicos de un medicamento no pueden ser comparados directamente a los rangos en los ensayos clínicos de otro medicamento, además de que podrían no reflejar los rangos observados en la práctica.
En ensayos controlados y no controlados en pacientes con DMD, 222 pacientes hombres con edad de 6 años y en adelante fueron tratados con DUVYZAT, incluyendo 210 pacientes tratados por ≥ 6 meses, 187 pacientes por ≥ 12 meses, y 105 pacientes por ≥ 24 meses.
El perfil de seguridad de DUVYZAT se basa en un estudio doble ciego, controlado con placebo, de 18 meses de duración, en un total de 179 pacientes ambulatorios con DMD a partir de los 6 años de edad que recibieron tratamiento simultáneo con corticosteroides (estudio 1) [vea Estudios clínicos (14)]. La dosis del estudio 1 se basó en el peso [vea Dosis y administración (2.2)]. Los pacientes eran excluidos del estudio si tenían las siguientes anomalías en la visita de selección: conteos de plaquetas, glóbulos blancos o de hemoglobina menores que el límite inferior del intervalo normal, triglicéridos en ayunas >300 mg/dl (3.42 mmol/l), o que tenían un intervalo QTc al inicio, corrección de Fridericia (QTcF) de >450 ms (promedio de 3 lecturas consecutivas con 5 minutos de diferencia) o antecedentes de factores de riesgo adicionales para Torsade de Pointes (por ejemplo, insuficiencia cardíaca, hipopotasemia, o antecedentes familiares de síndrome del intervalo QT prolongado). En general, el 2 % de los pacientes interrumpieron su participación en el estudio debido a reacciones adversas.
Tabla 3. Reacciones adversas reportadas en >5% de los pacientes tratados con DUVYZAT y en al menos 5% más que el placebo en el estudio 1
Reacción Adversa | DUVYZATN=118% | PlaceboN=61% |
| Diarrea | 37 | 20 |
| Dolor abdominal | 34 | 25 |
| Trombocitopenia1 | 33 | 0 |
| Nauseas/vómitos | 32 | 18 |
| Hipertrigliceridemia | 23 | 7 |
| Pirexia | 13 | 8 |
| Mialgia | 9 | 3 |
| Erupción | 9 | 2 |
| Artralgia | 8 | 2 |
| Fatiga | 8 | 0 |
| Estreñimiento | 7 | 2 |
| Disminución del apetito | 7 | 0 |
1La trombocitopenia incluye disminución de conteo de plaquetas y trombocitopenia
Reacciones adversas menos frecuentes en el estudio 1
Se presentaron reacciones adversas de hipotiroidismo y/o aumento de la hormona estimulante de la tiroides (THS, por sus iniciales en inglés) en el 5% de los pacientes tratados con DUVYZAT comparado con el 2% de los pacientes que recibieron el placebo.
7. INTERACCIONES CON EL MEDICAMENTO
7.1 Efecto de DUVYZAT en otros medicamentos
Sustratos sensibles a CYP3A4
Givinostat es un inhibidor intestinal débil de CYP3A4 [vea Farmacología clínica (12.3)]. Monitoree atentamente cuando tome DUVYZAT en combinación con sustratos orales sensibles a CYP3A4, para los cuales un pequeño cambio en la concentración de plasma del sustrato puede causar toxicidades severas.
Sustratos sensibles a OCT2
Givinostat es un inhibidor débil del transportador de captación renal OCT2 [vea Farmacología clínica (12.3)]. Monitoree atentamente cuando tome DUVYZAT en combinación con medicamentos conocidos como sustratos sensibles al transportador OCT2, para los cuales una pequeña cantidad de concentración de plasma puede causar toxicidades severas.
7.2 Efecto de otros medicamentos en DUVYZAT
Evite el uso simultáneo de DUVYZAT con otros productos que tengan potencial para prolongar el intervalo QTc. Si no se puede evitar el uso simultáneo, obtenga electrocardiogramas al inicio, durante el uso simultáneo, y como se indique clínicamente [vea Advertencias y Precauciones (5.4)]. Suspenda DUVYZAT si el intervalo QTc es > 500 ms o el cambio desde el inicio es > 60 ms [vea Dosis y administración (2.1)].
DUVYZAT causa prolongación del intervalo QTc [vea Farmacología clínica (12.3)]. El uso simultáneo de DUVYZAT con otros productos que prolongan el intervalo QTc puede resultar en un gran incremento del intervalo QTc y reacciones adversas asociadas a la prolongación del intervalo QTc, incluyendo Torsade de Pointes, otras arritmias severas, y muerte repentina [vea Advertencias y Precauciones (5.4)].
8. USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
Resumen de riesgos
DUVYZAT es recetado para el tratamiento de la DMD, la cual es una enfermedad predominante en pacientes hombres jóvenes. Por esta razón, no hay datos correctos disponibles para evaluar el uso de DUVYZAT en mujeres embarazadas. En estudios realizados en animales, la administración oral de givinostat durante la organogénesis resultó en la disminución del peso corporal del feto y en un aumento de las variaciones estructurales; la administración oral durante el embarazo y la lactancia resultó en un aumento de la mortalidad embriofetal y de las crías, así como cambios neuroconductuales en las crías. En la población general de EE. UU., el riesgo de origen estimado de defectos por nacimiento mayores y abortos espontáneos en embarazos reconocidos clínicamente es del 2 al 4% y del 15 al 20%, respectivamente.
Datos
Datos de animales
La administración oral de givinostat (0, 40, ó 160 mg/kg/por día) a ratas embarazadas a lo largo de la organogénesis resultó en una reducción del peso corporal del feto con la dosis más alta evaluada, y un aumento de la incidencia de las variaciones esqueléticas y viscerales en las dosis media y alta. La dosis sin efecto (40 mg/kg/por día) para los efectos adversos en el desarrollo embriofetal se asoció con exposiciones al plasma materno (área bajo la curva, [AUC, por sus iniciales en inglés]) más bajas que la de los humanos con la dosis más alta recomendada (MRHD, por sus iniciales en inglés) de 53.2 mg dos veces al día.
La administración oral de givinostat (0, 40, 80, o 160 mg/kg/por día) a conejas embarazadas a lo largo de la organogénesis resultó en la muerte materna con la dosis más alta evaluada, teniendo muy pocos fetos para evaluar. No se observaron efectos adversos en el desarrollo embriofetal en las dosis baja y media. Las exposiciones al plasma (AUC) con la dosis sin efecto más alta (80 mg/kg) para los efectos adversos en el desarrollo embriofetal fueron aproximadamente 4 veces más altas en los humanos con la MRHD.
La administración oral de givinostat (0, 40, 80, o 160 mg/kg/por día) a ratas a lo largo de todo el embarazo y la lactancia resultó en aumentos de la mortalidad embriofetal, nacimientos sin vida, y mortalidad de las crías con la dosis más alta evaluada. Cuando las crías se evaluaron después del destete (día postnatal 49), se observaron efectos adversos en el comportamiento (disminución de la actividad al aire libre) con todas las dosis. No se identificó dosis sin efecto para efectos adversos del desarrollo, las exposiciones al plasma (AUC) con la dosis más baja evaluada fueron más bajas que en los humanos con la MRHD.
8.2 Lactancia
Resumen de riesgos
No hay datos en humanos ni animales que evalúen el efecto de DUVYZAT o sus metabolitos en la producción de leche, la presencia de givinostat en la leche, o los efectos de dar leche al lactante. Los beneficios de dar leche materna en el desarrollo y la salud deben ser considerados junto con la necesidad clínica de la mamá de tomar DUVYZAT y cualquier efecto adverso posible en el lactante causado por DUVYZAT o por una condición materna subyacente.
8.3 Potencial reproductivo de mujeres y hombres
No hay ningún dato humano disponible sobre el efecto de DUVYZAT en el potencial reproductivo.
Los estudios en animales indican posibles efectos adversos en la reproducción [vea Toxicología no clínica (13.1)].
8.4 Uso pediátrico
La seguridad y efectividad de DUVYZAT en niños de 6 años de edad y en adelante ya se han establecido [vea Estudios clínicos (14)], pero seguridad y efectividad en pacientes pediátricos de menos de 6 años no se han establecido.
Datos en animales jóvenes
En un estudio de ratas hembras y machos jóvenes, givinostat se administró de forma oral en dosis de 0, 10, 20, ó 40 mg/kg en los días postnatales (PND, por sus iniciales en inglés) 7 al 2, en dosis de 0, 15, 30, ó 60 mg/kg por día en PNDs 28 al 48, y en dosis de 0, 15, 45, ó 9’ mg/kg/por día en PNDs 49 al 92. Se observaron efectos adversos en el comportamiento (aumento de actividad locomotora y disminución de la inhibición prepulso del sobresalto auditivo) con la dosis alta al final del periodo de dosificación. Los efectos adversos en la actividad locomotora, pero no en la inhibición prepulso, se observaron al final del periodo de recuperación principalmente con las dosis media y alta. Las disminuciones persistentes en la densidad de los huesos se observaron con las dosis evaluadas. No se identificó una dosis sin efecto para efectos adversos en el desarrollo postnatal, la dosis más baja evaluada se asoció con exposiciones al plasma (AUC) más bajas que las de los humanos con la MRHD.
8.5 Uso geriátrico
La DMD es en su mayoría una enfermedad en niños y adultos jóvenes; por esta razón, no hay experiencia del uso de DUVYZAT en pacientes con DMD geriátricos.
8.6 Insuficiencia hepática
No se llevó a cabo un estudio clínico dedicado a evaluar la farmacocinética de DUVYZAT en sujetos con insuficiencia hepática, por lo que no se puede hacer una recomendación en el ajuste de dosis para pacientes con insuficiencia hepática. Debido a que DUVYZAT se elimina principalmente a través del metabolismo hepático, se espera que la insuficiencia hepática aumente la exposición a givinostat [vea Farmacología clínica (12.3)].
11. DESCRIPCIÓN
La suspensión oral de DUVYZAT (givinostat) contiene clorhidrato monohidratado de givinostat, un inhibidor de la histona deacetilasa. El clorhidrato monohidratado de Givinostat se designa químicamente como: [6-(dietilaminometil)naftalen-2 il]metil[4(hidroxicarbamoil) fenil] clorhidrato monohidratado de carbamato. La fórmula molecular es C24H27N3O4•HCl•H2O y el peso molecular es 475.97 g/mol. Su fórmula estructural es:
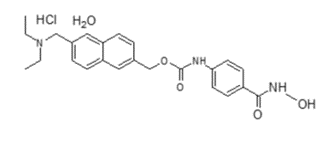
El clorhidrato monohidratado de givinostat es un polvo cristalino no higroscópico, de color blanco a blanquecino, que es de muy ligeramente a ligeramente soluble en medios acuosos y ligeramente soluble en etanol.
DUVYZAT contiene 8.86 mg/mL de givinostat (equivalente a 10 mg/L de de clorhidrato
monohidratado de givinostat), así como los siguientes ingredientes no activos: sabor a crema, glicerina, solución de sorbitol no cristalizante, sabor a durazno, polisorbato 20, agua purificada, sacarina sódica, benzoato de sodio, hidróxido de sodio, ácido tartárico y goma tragacanto.
12. FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de acción
DUVYZAT es un inhibidor de la histona deacetilasa. Se desconoce el mecanismo preciso por el cual DUVYZAT ejerce su efecto en pacientes que tienen DMD.
12.2 Farmacodinámica
Fracción de grasa muscular evaluada a través de espectroscopía por RM
El porcentaje de la fracción de grasa presente en el músculo vasto lateral (MVL, por sus iniciales en inglés) del muslo se midió en el estudio 1 [vea Estudios clínicos (14)] usando espectroscopía por resonancia magnética. A los 18 meses, para los pacientes con fracción de grasa en el MVL al inicio dentro del rango del >5% a ≤30%, un promedio de aumento (diferencia absoluta de los niveles del punto de inicio) de la fracción de grasa en el VLM fue del 7.48% en los pacientes tratados con DUVYZAT, comparados con un 10.89% de aumento en los pacientes que recibieron el placebo.
Electrofisiología cardiaca
El aumento más grande en el intervalo QTc de 13.6 ms (intervalo de confianza superior de 17.1 ms) se produjo 5 horas después de la administración de givinostat de 265.8 mg a sujetos sanos (aproximadamente 5 veces la dosis recomendada de 53.2 para pacientes con DMD que pesaban 60 kg o más) [vea Advertencias y precauciones (5.4)].
12.4 Farmacocinética
Givinostat exhibe una cinética linear con el rango de dosis estudiado. La exposición sistemática a givinostat fue proporcional a la dosis a lo largo del rango de dosis terapéutico. Las concentraciones en equilibrio estacionario se alcanzan dentro de los 5 a 7 días después de la dosis doble diaria. Se observó una acumulación de menos del doble para givinostat después de la administración doble diaria.
Absorción
No se determinó la biodisponibilidad absoluta. El tiempo de las concentraciones al plasma máximas es de alrededor de 2 a 3 horas después de la administración oral.
Efecto de la comida
Una comida con alto estándar de grasa resultó en un aumento de la exposición (cerca de un aumento del 40% en el área AUC y cerca de un incremento del 23% en la concentración máxima de plasma (Cmax) y un retraso en el tiempo de concentración máxima (Tmax) de 2 a 3 horas [vea Dosis y administración (2.2)].
Distribución
Givinostat está aproximadamente vinculado en un 96% a las proteínas plasmáticas humanas y está ligeramente dividido en células de la sangre (proporción de sangre en el plasma = 1.3).
Eliminación
En el plasma, la eliminación de media vida de givinostat es de alrededor de 6 horas.
Metabolismo
Estudios in vitro con preparaciones enzimáticas humanas junto con metabolismo animal mostró que givinostat está metabolizado de forma extensiva formando varios metabolitos. El CYP450 y las uridina difosfato glucuronosiltransferasas (UGT, por sus iniciales en inglés) no están involucrados en las reacciones metabólicas principales. Cuatro metabolitos mayores, los cuales no están activos con respecto a la eficacia de givinostat, se han caracterizado en humanos y especias preclínicas.
Excreción
La eliminación de givinostat es probablemente dependiente del metabolismo, seguida de una excreción biliar y renal de los metabolitos resultantes, como lo sugirió el estudio de equilibrio de masas en ratas. La excreción urinaria de givinostat en humanos es mínima (<3% de la dosis).
Poblaciones específicas
Los análisis de población de farmacocinética (PK, por su abreviatura en inglés) de givinostat pueden verse afectados por el peso corporal, mientras que la edad no tiene efectos en la farmacocinética de givinostat.
Pacientes con insuficiencia hepática
La farmacocinética y seguridad de givinostat no han sido estudiadas en pacientes con insuficiencia hepática. El givinostat es altamente metabolizado y, por ello, el impacto de la insuficiencia hepática en la exposición de givinostat no se puede excluir [vea Uso en poblaciones específicas (8.6)].
Pacientes con insuficiencia renal
La farmacocinética y seguridad de givinostat no han sido estudiadas en pacientes con insuficiencia renal. Sin embargo, se espera que la insuficiencia renal no impacte la exposición de givinostat debido a que la excreción renal no es una ruta significativa de eliminación de givinostat.
Estudios de interacción del medicamento
In vitro
Givinostat no es un sustrato de las enzimas del citocromo P450 (CYP450) ni de la UGT. Por lo tanto, la coadministración de medicamentos que son inductores o inhibidores de las enzimas metabolizadoras principales no afectará significativamente la exposición sistémica del givinostat.
Se investigaron el givinostat y sus metabolitos ITF2374, ITF2375, ITF2440 e ITF2563 como inhibidores de las principales subfamilias del CYP450, y los resultados indicaron que no se espera inhibición de CYP1A2, 2C9, 2C19, 2D6, 2B6, 2C8 ni 3A4. Givinostat mostró inducción de CYP1A2, 2B6 y CYP3A4.
Estudios in vitro indican que givinostat es un sustrato de los transportadores intestinales: la glucoproteína P (gp-P) y la proteína de resistencia al cáncer de mama (BCRP, por sus iniciales en inglés). Givinostat mostró el potencial para inhibir los transportadores intestinales gp-P (MDR1) y la BCRP basado en los resultados in vitro. Sin embargo, no se espera que estas interacciones sean clínicamente significativas.
In vivo
Se observó una inhibición débil del transportador de captación renal OCT2 por parte del givinostat en los ensayos clínicos por las medidas de creatinina (subestado de OCT2) [vea Interacciones con el medicamento (7.1)].
Se llevó a cabo una interacción clínica del medicamento en voluntarios sanos para evaluar los efectos de la coadministración de givinostat con otros medicamentos y los resultados indicaron que:
- givinostat tiene una inhibición débil de la enzima CYP3A4 intestinal basada en la exposición de un sustrato de CYP3A4, midazolam, [vea Interacciones con el medicamento (7.1)].
- givinostat probablemete no inhibe transportadores P-gp basados en la exposición de dabigatrán
- Los inhibidores fuertes P-gp tienen un efecto débil en givinostat basado en la exposición de claritromicina, la cual tuvo un incremento de la Cmax de alrededor del 40% sin un cambio significativo del AUC.
El efecto de los inhibidores de la BCRP en la PK de givinostat no se ha estudiado en un estudio clínico. Sin embargo, se espera que el efecto de los inhibidores de la BCRP en la PK de givinostat sea menos en los inhibidores P-go basados en la comparación de los cocientes de eflujo mediados por los dos transportadores determinados en los modelos celulares in vitro.
13. TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogenesis, mutagenesis, y deterioro de la fertilidad
Carciogenesis
No se han llevado a cabo estudios para evaluar el potencial carcinogénico de givinostat.
Mutagenesis
Givinostat resultó positivo en un ensayo de mutación bacteriana inversa (Ames), y negativo en un ensayo de mutación de células de mamíferos in vitro (linfoma de ratón), un ensayo de aberración cromosómica in vitro en células de mamíferos (linfocitos humanos), y en un ensayo de mutación genética in vivo (con parámetros Pig-a) en ratas transgénicas Big Blue.
Deterioro de la fertilidad
La administración oral de givinostat (0, 40, 80, ó 160 mg/kg) previo a y a lo largo del apareamiento en ratas machos y hembras, y continuando al día 7 de gestación en hembras, resultó en ningún efecto adverso en la fertilidad. No obstante, hubo un aumento en los cuerpos lúteos con las dosis media y alta, y un aumento en la pérdida previa y posterior a la implantación con todas las dosis. No se identificó una dosis sin efecto para efectos adversos en el desarrollo embrionario temprano; las exposición de plasma (AUC) con la dosis más baja evaluada fueron más bajas que la de los humanos con la dosis humana máxima recomendada de 53.2 mg dos veces al día.
14. ESTUDIOS CLÍNICOS
La efectividad de DUVYZAT para el tratamiento de la distrofia muscular de Duchenne (DMD) se evaluó en un estudio aleatorizado, doble ciego, controlado con placebo, con 18 meses de duración (estudio 1; NCT02851797). Un total de 179 pacientes fueron aleatorizados en la proporción 2:1 para recibir ya fuera DUVYZAT (n=118) o placebo (n=61). Se aplicó un régimen de dosis basado en el peso [vea Dosis y administración (2.2)]. El estudio incluyó pacientes hombres de 6 años de edad y en adelante con un diagnóstico confirmado de DMD que eran ambulatorios y con una dosis estable de corticosteroides. En el inicio, los pacientes tenían un promedio de edad de 9.8 años, 90% eran blancos, 3% eran asiáticos, 3% eran negros.
El parámetro principal fue el cambio del punto de inicio al mes 18 en la prueba de tiempo para subir 4 escalones (4SC, por su abreviatura en inglés) para DUVYZAT en comparación con el placebo. La prueba de 4SC es una medida de la función muscular que evalúa el tiempo que toma subir 4 escalones. Un parámetro de eficacia secundario fue el cambio del punto de inicio al mes 18 en la función física como la evalúa la escala ambulatoria North Star (NSAA, por sus siglas en inglés).
El análisis principal de la población se basó en un rango pre específico de la fracción muscular de inicio como se determinó por la espectroscopía por RM. Los pacientes tratados con DUVYZAT mostraron estadísticamente significativa menos disminución en la prueba de 4SC comprado con el placebo (vea Tabla 4). Los pacientes tratados con givinostat experimentaron menos agravamiento en la NSAA comparados con el placebo, lo cual fue nominal, pero no estadísticamente significativo, según el ajuste de multiplicidad preespecífico.
Tabla 4. Cambio desde el punto de inicio al mes 18 en la prueba de tiempo para subir 4 escalones (4SC) en comparación con el placebo*
| Punto de inicio promedio de la prueba 4SC (segundos) | Cambio promedio desde el punto de inicio | Diferencia del tratamiento respecto al placebo (IC del 95%) | Valor de p | |
| DUVYZAT(n=81) | 3.39 | 1.25 | -1.78(-3.46, -0.11) | 0.037 |
| Placebo(n=39) | 3.48 | 3.03 |
16. FORMATO/ALMACENAMIENTO Y MANEJO
16.1 FORMATO
La suspensión oral DUVYZAT (givinsotat) es una suspensión de color blanco a blanquecino o ligeramente rosa, con sabor a durazno con crema. Se presenta en un envase ámbar de tereftalato de polietileno cerrado con una tapa de rosca de polietileno de alta densidad, a prueba de niños, con un adaptador de jeringa de polietileno de baja densidad, que contiene 140 ml de suspensión oral (NDC 11797-110-01). Cada ml contiene 8.86 mg de givinostat.
DUVYZAT se presenta en una caja de cartón, NDC 1197-110-02, que contiene:
- un envase que contiene 140 ml de suspensión oral
- una jeringa oral graduada de 5 ml
- Información de receta e Instrucciones de uso
La Guía del medicamento se encuentra disponible en www.duvyzat.com/medication-guide
16.2 Almacenamiento y manejo
Mantener a una temperatura de 20°C a 25°C (de 68°F a 77°F), se permiten excursiones de 15°C a 30°C (de 59°F a 86°F) [vea Temperatura Ambiente Controlada de la USP]. No congelar. Mantener envase boca arriba.
Deseche cualquier cantidad de DUVYZAT sin usar que le haya quedado tras 60 días de haber abierto el envase.
17. INFORMACIÓN DE ASESORAMIENTO DEL PACIENTE
Aconseje al paciente leer la etiqueta para el paciente aprobada por la FDA (Guía del Medicamento e Instrucciones de uso).
Instrucciones de administración
Indique a los pacientes o proveedores de cuidado que vean la sección Dosis y Administración (2.4):
- Agite bien la suspensión oral DUVYZAT antes de medir cada dosis.
- Administrar usando la jeringa oral graduada que se incluye para medir el volumen apropiado de suspensión correspondiente a la dosis recetada para el paciente.
- Tome DUVYZAT con alimentos.
- Deseche cualquier cantidad de DUVYZAT sin usar que le haya quedado tras 60 días de haber abierto el envase.
Cambios hematológicos
Informe a los pacientes o proveedores de cuidado que DUVYZAT puede causar cambios hematológicos incluyendo disminución en el conteo de plaquetas (trombocitopenia), anemia, y una disminución en los neutrófilos (neutropenia) [vea Advertencias y precauciones (5.1)]. Comente a los pacientes que notifiquen a su proveedor de cuidado de la salud si presentan algún signo o síntoma de estas reacciones adversas (por ejemplo, facilidad para desarrollar moretones, sangrado excesivo por cortaduras, sangre en las heces, fatiga). Indique a los pacientes adherirse a las evaluaciones recomendadas para monitorear estas reacciones adversas. Informe a los pacientes que su dosis puede necesitar ser cambiada o su tratamiento podría ser suspendido, dependiendo de los resultados de sus pruebas de conteo de plaquetas.
Triglicéridos elevados
Informe a los pacientes y/o proveedores de cuidado que DUVYZAT puede causar un aumento de triglicéridos [vea Advertencias y precauciones (5.2)]. Informe a los pacientes que su dosis puede necesitar ser cambiada o su tratamiento podría ser suspendido, dependiendo de los resultados de sus pruebas de triglicéridos.
Problemas gastrointestinales
Informe a los pacientes o proveedores de cuidado que DUVYZAT puede causar diarrea y vómito, lo cual podría requerir medicamento para el tratamiento [vea Advertencias y precauciones (5.3)]. Indique a los pacientes que se mantengan hidratados si la diarrea o vómito se presenta, y contacten a su proveedor de cuidado de la salud si los síntomas persisten o son de moderados a severos. Informe a los pacientes que su dosis puede necesitar ser cambiada o su tratamiento podría ser suspendido, dependiendo de la severidad de la diarrea.
Prolongación del intérvalo QTc
Informe a los pacientes o proveedores de cuidado de la salud que DUVYZAT puede causar prolongación del intervalo QTc [vea Advertencias y precauciones (5.4)]. Indique a los pacientes que notifiquen a su proveedor de cuidado de la salud si presentan o desarrollan cualquier síntoma de prolongación del intervalo QTc significativo (por ejemplo, mareos, aturdimiento, síncope) o algún problema cardiaco nuevo, así como antes de tomar cualquier medicamento de venta libre (como difenhidramina), suplemento herbal (como equinácea), o medicamentos recetadas (como antibióticos).
Manufacturado por:
Italfarmaco S.A.
Madrid, España
Distribuido por:
ITF Therapeutics, LLC
Concord, MA 01742
DUVYZAT es una marca comercial propiedad de Italfarmaco S. p. A.
Todos los derechos reservados.
| GUÍA DEL MEDICAMENTODUVYZAT™ (doo’ vi zat)(givinostat)Suspensión oral |
| ¿Cuál es la información más importante que debo saber sobre DUVYZAT?DUVYZAT puede causar efectos secundarios serios incluyendo:Conteo de plaquetas bajo en la sangre (trombocitopenia). Las plaquetas son importantes para la coagulación de sangre, por lo que tener pocas puede aumentar el riesgo de sangrado y de moretones. Su proveedor de cuidado de la salud revisará su conteo sanguíneo antes de comenzar a tomar DUVYZAT, así como de manera regular durante el tratamiento para ver signos de trombocitopenia. Llame a su proveedor de cuidado de la salud inmediatamente si nota sangrado inusual o pequeñas marcas rojas o moradas en la piel llamadas petequias. Su proveedor de cuidado de la salud puede cambiar su dosis de DUVYZAT si su conteo de plaquetas en la sangre continúa estando bajo, o puede interrumpir su tratamiento con DUVYZAT. Niveles elevados de grasa (triglicéridos) en su sangre. Podría no presentar ningún síntoma, por lo que su proveedor de cuidado de la salud realizará pruebas de sangre antes de que empiece a tomar DUVYZAT, así como de manera regular durante el tratamiento para revisar sus niveles de triglicéridos. Su proveedor de cuidado de la salud puede cambiar su dosis de DUVYZAT si sus niveles de triglicéridos continúan estando altos, o puede interrumpir su tratamiento con DUVYZAT. Heces acuosas (diarrea) y vómitos frecuentes. DUVYZAT puede causar vómito y diarrea de moderada a severa. Si hay diarrea, debe mantener un registro de la frecuencia y severidad de sus síntomas, beber suficientes líquidos, y contactar a su proveedor de cuidado de la salud. Su proveedor de cuidado de la salud puede cambiar su dosis de DUVYZAT si la diarrea no se puede controlar o no se le quita. Su proveedor de cuidado de la salud puede interrumpir su tratamiento con DUVYZAT. |
| ¿Qué es DUVYZAT?DUVYZAT es una medicina recetada para el tratamiento de la distrofia muscular de Duchenne (DMD) en personas a partir de los 6 años y en adelante. No se sabe si DUVYZAT es segura y efectiva en menores de 6 años. |
| Antes de tomar DUVYZAT, informe a su proveedor de cuidado de la salud de todas sus condiciones médicas, incluyendo si usted:tiene cualquier problema en el corazón o toma algún medicamento que pudiera incrementar las probabilidades de ritmo cardíaco irregular. tiene cualquier problema de sangrado.Informe a su doctor sobre todas las medicinas que toma, incluyendo las que son con receta, de venta libre, vitaminas, y suplementos herbales. Tomar DUVYZAT junto con ciertas medicinas puede afectar una a la otra, además de que puede causar efectos secundarios serios. No empiece o deje de tomar otras medicinas sin hablarlo con su proveedor de cuidado de la salud. Conozca las medicinas que toma. Tenga a la mano una lista con ellas para mostrarsela a su proveedor de cuidado de la salud y farmaceuta cuando empiece a tomar una nueva. |
| ¿Cómo debo tomar DUVYZAT?Revise las Instrucciones de uso que vienen con su medicina DUVYZAT para ver las instrucciones detalladas sobre cómo tomar DUVYZAT de la manera correcta. Tome DUVYZAT por la boca con alimentos. Tome DUVYZAT exactamente como lo recetan. Su proveedor de cuidado de la salud le dirá cuánto DUVYZAT tomar y cuándo tomarlo.Su proveedor de cuidado de la salud puede cambiar su dosis de DUVYZAT si es necesario. No cambie su dosis de DUVYZAT sin hablarlo con su proveedor de cuidado de la salud. Agite la botella por al menos 30 segundos: ponga la botella boca abajo y boca arriba de manera continua. Deténgase cuando la suspensión de DUVYZAT se vea uniforme por dentro. Tome la dosis recetada de DUVYZAT por la boca (de manera oral) usando la jeringa oral que viene con su medicina DUVYZAT. No se deshaga de la jeringa oral. DUVYZAR no debe mezclarse con agua u otros líquidos. Si se le olvida tomarse una dosis de DUVYZAT, déjela pasar y tome su siguiente dosis de DUVYZAT como está programada. |
| ¿Cuáles son los posibles efectos secundarios de DUVYZAT?DUVYZAT puede causar efectos secundarios serios, incluyendo:vea la sección “¿Cuál es la información más importante que debo saber sobre DUVYZAT?”cambios en la actividad eléctrica de su corazón llamada prolongación del QT. La prolongación del QT puede elevar el riesgo de desarrollar un tipo de ritmo cardíaco irregular conocido como Torsades de Pointes. Llame a su proveedor de cuidado de la salud inmediatamente si presenta desmayos, ritmo cardíaco irregular, se siente mareado, o pierde el conocimiento.Los efectos secundarios más comunes de DUVYZAT incluyen:heces acuosas o sueltasnauseas conteo bajo de plaquetas en la sangreniveles altos de grasa en la sangrevómitodolor de estómago (abdominal)fiebre Diga a su proveedor de cuidado de la salud si presenta algún efecto secundario que le moleste o que no se le quite. Éstos no son todos los efectos secundarios posibles de DUVYZAT. Para mayor información, pregunte a su proveedor de cuidado de la salud o farmaceuta. Llame a su doctor para recibir un mayor asesoramiento médico sobre los efectos secundarios, los cuales también puede reportar a la FDA al 1-800-FDA-1088. |
| Información general sobre el uso seguro y efectivo de DUVYZATLas medicinas son recetadas a veces con propósitos diferentes a los que se enlistan en la Guía del Medicamento. No use DUVYZAT en una condición para la que no ha sido recetado. No dé DUVYZAT a otras personas, incluso si presentan los mismos síntomas que usted. Podría hacerles daño. Puede preguntar a su farmaceuta o proveedor de cuidado de la salud para más información sobre DUVYZAT que se escribe para los profesionales del cuidado de la salud. |
| ¿Cuáles son los ingredientes de DUVYZAT?Ingrediente activo: givinostatIngredientes inactivos: sabor a crema, glicerina, solución de sorbitol no cristalizante, sabor a durazno, polisorbato 20, agua purificada, sacarina sódica, benzoato de sodio, hidróxido de sodio, ácido tartárico, goma tragacanto. |

